美国
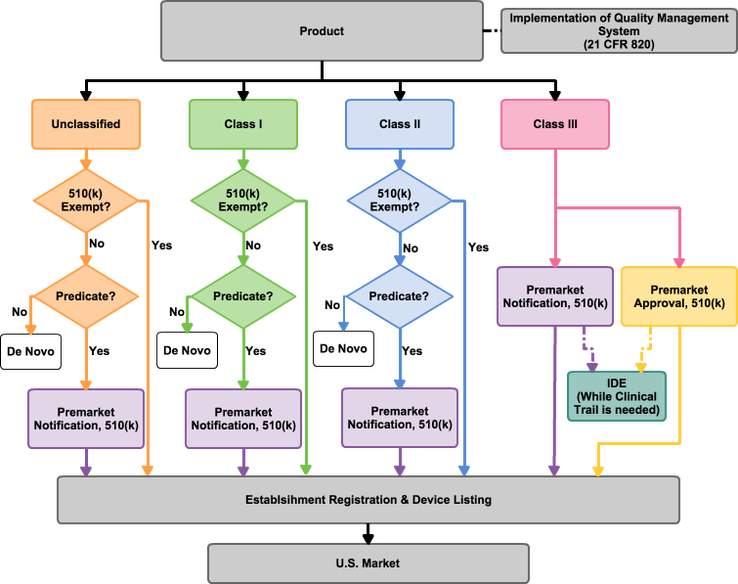
对要进入美国市场的医疗器材,产品必须要依据美国食品药品监督管理局(FDA)的规范进行分类,分类成无分级(Unclassified)、第一级、第二级、第三级。每一级别的医疗器材可以归类到对应的产品分类编号并借此了解所需遵循的法规。要在美国进行医疗器材贩售,厂商需要取得许可或核准。大多数的第二级医疗器材需要通过上市前通知510(k),而第三级的医疗器材则是依照产品分类编号来决定需要申请上市前通知510(k)还是要申请上市前核准(PMA )。正常来说只有少数510(k)以及多数PMA在申请过程中会需要用到临床报告佐证产品的安全和有效。要进行临床试验,实验的步骤和手续要经过临床试验计画书申请(IDE)来核查后才能进行。一旦提交充足的资料报告并通过美国食品药品监督管理局的审查后,美国食品药品监督管理局会给予上市许可或核准。
510(k)是上市前所需进行的FDA申请,为的是向美国食药局证明器材在安全性和有效性上与现在合法市场上贩售的器材是实质相等的。由于510(k)是基于实质相等性来申请的,寻找相似的医疗器材是非常重要的。相对来说上市前许可的模式则是著重于医疗器材本身的安全性以及有效性。不同的申请方法要求申请人提出不同文件,弘亚能够协助我们的客户以效率并且经济的方式来准备资料、撰写报告。取得上市许可或核准后,厂商可以进行公司注册和产品列名。如果是免除510(k)和PMA的第一级医疗器材则是只要完成公司注册和产品列名即可上市贩卖。依据美国食品药品监督管理局规定,国外厂商需要指定一个美国代理人作为美国食品药品监督管理局和厂商间联络的窗口。
弘亚生技顾问有限公司有着多年协助客户进入美国市场的法规咨询和品质系统辅导经验,我们辅导客户准备并申请公司注册、产品列名、上市前通知510(k)、上市前核准(PMA) 、以及临床试验计画书申请。欢迎联络我们任何关于进入美国医疗器材市场的问题。
510(k)是上市前所需进行的FDA申请,为的是向美国食药局证明器材在安全性和有效性上与现在合法市场上贩售的器材是实质相等的。由于510(k)是基于实质相等性来申请的,寻找相似的医疗器材是非常重要的。相对来说上市前许可的模式则是著重于医疗器材本身的安全性以及有效性。不同的申请方法要求申请人提出不同文件,弘亚能够协助我们的客户以效率并且经济的方式来准备资料、撰写报告。取得上市许可或核准后,厂商可以进行公司注册和产品列名。如果是免除510(k)和PMA的第一级医疗器材则是只要完成公司注册和产品列名即可上市贩卖。依据美国食品药品监督管理局规定,国外厂商需要指定一个美国代理人作为美国食品药品监督管理局和厂商间联络的窗口。
弘亚生技顾问有限公司有着多年协助客户进入美国市场的法规咨询和品质系统辅导经验,我们辅导客户准备并申请公司注册、产品列名、上市前通知510(k)、上市前核准(PMA) 、以及临床试验计画书申请。欢迎联络我们任何关于进入美国医疗器材市场的问题。