中国
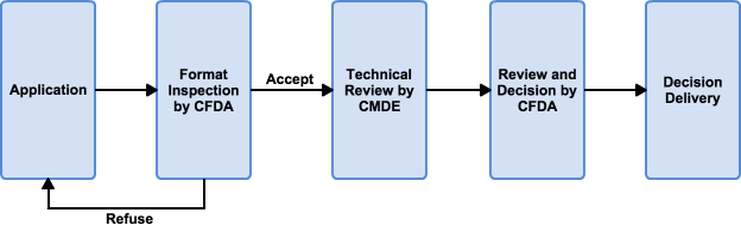
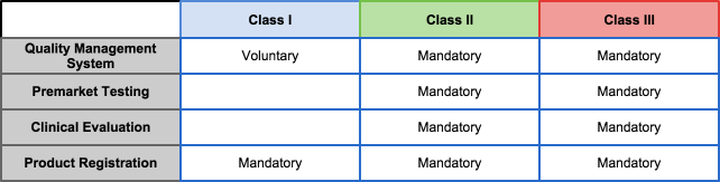
准备进入中国市场的医疗器材厂商,必须要符合并通过中国国家食品药物监督管理总局(CFDA)的相关法律规范。这些规范是依据【医疗器械监督管理条例】与【医疗器械注册管理办法】所架构的,类似于其他国家,中国食药监管总局将医疗器材根据风险程度、使用方式、适应症等归类为第一类、第二类、第三类,等级越高危险性越大。所有类别的医疗器械上市前都需要经过中国食药监管总局审视、认可并给予注册认证。申请过程中所需的检验与临床报告并需要在中国政府认证的检验机构或实验室进行。对于输入中国的医疗器械,第一次进行注册可以归类为三类:
根据这三种情况,厂商需要于申请过程中提供不同的文件报告来支持产品对宣称之适应症的安全性以及有效性。此外,中国食药监管总局要齐所有境外医疗器械厂商只派一个注册过的正式中国代理人作为与中国食药监管总局沟通联络的窗口。在提交充足的产品安全性跟有效性的报告文件并通过中国食药监管总局审查后,中国食药监管总局将会给予为期五年的上市许可执照。弘亚生技协助客户准备申请上市许可执照所需的文件并提供中国代理人的服务。有任何关于进入中国市场上的疑问,欢迎联络我们进行询问。
- 已获得境外医疗器械上市许可的境外医疗器械
- 未获得境外医疗器械上市许可的第一类境外医疗器械
- 未获得境外医疗器械上市许可的第二、三类境外医疗器械
根据这三种情况,厂商需要于申请过程中提供不同的文件报告来支持产品对宣称之适应症的安全性以及有效性。此外,中国食药监管总局要齐所有境外医疗器械厂商只派一个注册过的正式中国代理人作为与中国食药监管总局沟通联络的窗口。在提交充足的产品安全性跟有效性的报告文件并通过中国食药监管总局审查后,中国食药监管总局将会给予为期五年的上市许可执照。弘亚生技协助客户准备申请上市许可执照所需的文件并提供中国代理人的服务。有任何关于进入中国市场上的疑问,欢迎联络我们进行询问。