台湾
无论台湾或海外公司要在台湾进行医疗器材与体外试剂贩卖,都需要符合台湾卫生福利部食品药物管理署的先关法规规范,食药署基于危险等级将医材分类为第一级、第二级以及第三级。台湾的分级规范类似于美国的分级系统,第一级为低分险之器材,第二级与第三级则是有较高风险,而不论是哪一等级在上市前皆须通过食药署的许可。
要取得上市许可,国外的医疗厂商需要指定一个在台湾本地的代表,来管理并进行产品注册过程并作为海外厂商和食药署的联络窗口。台湾代表需要有在台地址并且持有正式的药商许可执照,也负责在提交申请上市许可所需之档案。于申请的过程中,医疗器材厂商需要有品质系统文件(QSD)来证明制造过程符合美国的品质系统规范(QSR) 或是ISO 134850:2003。根据我们之前的经验,卫服部食药署较偏好ISO 13485:2003。一但经确认品质系统符合规范,食药署会给予国外厂商输入医疗器材品质系统文件(QSD)认可,此认可三年内有效。此外外国医疗器材厂商需要取得外国政府认证(CFG)来证明此器材先前已在海外贩售。 QSD与CFG都是外国厂商申请上市许可所需的必备文件。至于国内厂商不须这两份文件,但必须取得优良制造规范(GMP)以进行上市许可申请。
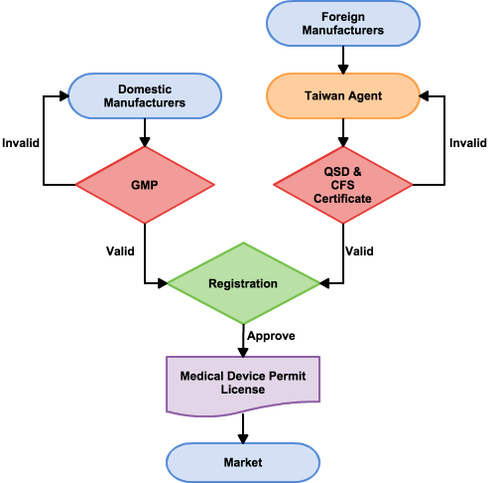
在取得这些认证文件后,就可以向食药署提出充足的资料来进行产品登记。厂商应该提交产品资讯、产品测试报告、临床报告(假如有需求)、以及其他产品相关文件。在国外进行之检测通常被食药署承认。在通过食药署的审核后,厂商可以取得医疗器材贩卖许可执照,可以开始进行贩售。医疗器材贩卖许可执照有效期为五年,如要更新请于过期前六个月提除申请,下面的流程图为简约的申请流程。弘亚生技帮助客户申请GMP、QSD、CFS、以及注册流程。
要取得上市许可,国外的医疗厂商需要指定一个在台湾本地的代表,来管理并进行产品注册过程并作为海外厂商和食药署的联络窗口。台湾代表需要有在台地址并且持有正式的药商许可执照,也负责在提交申请上市许可所需之档案。于申请的过程中,医疗器材厂商需要有品质系统文件(QSD)来证明制造过程符合美国的品质系统规范(QSR) 或是ISO 134850:2003。根据我们之前的经验,卫服部食药署较偏好ISO 13485:2003。一但经确认品质系统符合规范,食药署会给予国外厂商输入医疗器材品质系统文件(QSD)认可,此认可三年内有效。此外外国医疗器材厂商需要取得外国政府认证(CFG)来证明此器材先前已在海外贩售。 QSD与CFG都是外国厂商申请上市许可所需的必备文件。至于国内厂商不须这两份文件,但必须取得优良制造规范(GMP)以进行上市许可申请。
在取得这些认证文件后,就可以向食药署提出充足的资料来进行产品登记。厂商应该提交产品资讯、产品测试报告、临床报告(假如有需求)、以及其他产品相关文件。在国外进行之检测通常被食药署承认。在通过食药署的审核后,厂商可以取得医疗器材贩卖许可执照,可以开始进行贩售。医疗器材贩卖许可执照有效期为五年,如要更新请于过期前六个月提除申请,下面的流程图为简约的申请流程。弘亚生技帮助客户申请GMP、QSD、CFS、以及注册流程。